Seguimiento del paciente oncológico en tratamiento con quimio y/o radioterapia por parte del Médico de Familia
Tassone Olmo M
Especialista en MFyC. EAP centro de salud urbano. Mérida (Badajoz)
DOI: 10.82033/MEDFAMANDAL.2025.RR1556
Recibido el 04-06-2025, aceptado para publicación el 07-07-2025.Ver y descargar artículo en pdf
INTRODUCCIÓN
En España, el cáncer es una de las principales causas de morbi-mortalidad. El número de cánceres diagnosticados en España en el año 2024 se estima que alcanzará los 286.664 casos según los cálculos de REDECAN, lo que supone un ligero incremento con respecto al año 2023. Al igual que se espera un incremento en la incidencia del cáncer a nivel mundial en los próximos años, en España se estima que en 2040 la incidencia alcance unos 341.000 casos. Los cánceres más frecuentemente diagnosticados en España en 2024 serán los de colon y recto (44.294 nuevos casos), mama (36.395), pulmón (32.768), próstata (30.316) y vejiga urinaria (22.097). A mucha distancia, los siguientes cánceres más frecuentes serán los linfomas no hodgkinianos (10.706), y los cánceres de páncreas (9.986), riñón (9.208), cavidad oral y faringe (7.603), cuerpo uterino (7.305), estómago (6.868) e hígado (6.856) (1).
Dado al aumento del volumen de pacientes con cáncer que consultarán en atención primaria, por lo que además de factores preventivos de cribado y seguimiento del paciente largo superviviente es importante el conocimiento y manejo de los efectos secundarios de los tratamientos por parte del médico de familia.
La atención al paciente oncológico se ha centrado sobre todo en intervenciones altamente tecnológicas enfocadas a la enfermedad, con vistas a mejorar la supervivencia. Ahora se pone un énfasis cada vez mayor en el abordaje preventivo, el diagnóstico precoz, el cuidado del largo superviviente y la atención al final de la vida. En este nuevo enfoque, el médico de familia está llamado a desempeñar un papel crucial por su capacidad de proporcionar una atención integral, centrada en la persona, longitudinalidad y accesibilidad. El médico de familia sigue manteniendo una responsabilidad con su paciente y con su familia durante el periodo diagnóstico y tratamiento. El apoyo social y psicológico, el control de la comorbilidad y en ocasiones la atención urgente de los efectos agudos del tratamiento, están dentro de sus competencias (2).
TIPOS DE TRATAMIENTOS
Dentro de los tratamientos que reciben los pacientes oncológicos encontramos la quimioterapia, radioterapia, inmunoterapia, hormonoterapia.
*La quimioterapia: tiene la función de impedir la reproducción de células cancerosas pero debido a su poca especificidad afecta tanto a las células cancerígenas como a células sanas del organismo, sobre todo si se encuentran en división activa como por ejemplo las células de la médula ósea, tejido intestinal, folículos pilosos y sistema reproductor. Esto marcará gran parte de sus efectos secundarios (3).
*La hormonoterapia: las hormonas actúan como estimulantes del crecimiento de las células tumorales. Se utilizan fármacos que actúan sobre las hormonas para detener el avance del cáncer, bien sea evitando su síntesis o alterando sus efectos. Este tipo de tratamientos se emplean principalmente en los tumores de mama, próstata, endometrio, ovario o tumores neuroendocrinos (4).
*La inmunoterapia: las células cancerosas mediante la expresión de unas proteínas en su superficie bloquean los receptores específicos de los linfocitos T provocando una inactividad del sistema inmune hacia ellas al no ser reconocidas. La inmunoterapia facilita el bloqueo de dichas proteínas de superficie permitiendo la correcta actividad del sistema inmunitario. Es un tratamiento muy específico, con memoria inmunológica y provoca una acción prolongada. Puede prescribirse sola o combinada con otra inmunoterapia o quimioterapia (5).
*La terapia dirigida o terapia biológica bloquea de forma específica aspectos concretos de la biología celular o tumoral. Tienen gran selectividad por las células tumorales respecto al resto de las células de organismo por lo que tiene la capacidad de actuar contra el cáncer con menos efectos secundarios (6).
EFECTOS SECUNDARIOS Y VIGILANCIA
Como explican Blasco A y Caballero C (SEOM 2019), los efectos secundarios producen gran temor en los pacientes, que, aunque en la mayoría de los casos son más soportables de lo esperado, la toxicidad asociada al tratamiento de quimioterapia es un aspecto muy importante, principalmente por la influencia negativa que ejerce sobre la calidad de vida de los pacientes, así como el riesgo vital que puede suponer en algunas circunstancias.
Es por ello, que es importante conocer los posibles efectos secundarios para estar expectantes durante el seguimiento por parte del médico de familia de los pacientes que están en tratamiento como las posibles escuelas una vez finalizado dicho tratamiento. Tomamos un papel importante en la prevención de los efectos secundarios dando a los pacientes información y tratamiento de soporte para minimizar la gravedad.
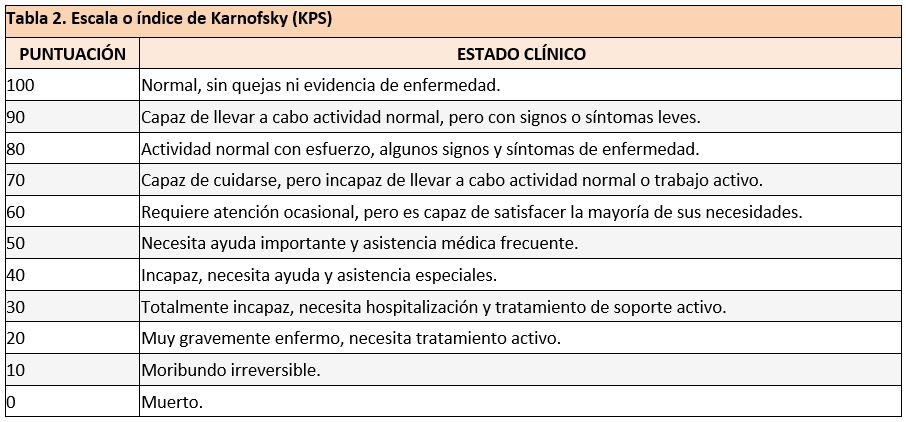
En los informes de los pacientes oncológicos se suele ver la escala ECOG (tabla 1) que valora la evolución de las capacidades del paciente en su vida diaria manteniendo al máximo su autonomía, es muy importante para valorar el planteamiento de ciertos tratamientos y se puede valorar la evolución del paciente a lo largo de las visitas. Así como la escala Karnofsky (tabla 2), que valora el estado funcional de pacientes tratados con quimioterapia.

En este artículo abordaremos los efectos secundarios relacionados con la quimioterapia y radioterapia.
TOXICIDADES MÁS COMUNES EN RELACIÓN AL TRATAMIENTO CON QUIMIOTERAPIA
Los efectos secundarios más comunes son los que aparecen de manera inmediata o precoz como son: la alopecia, náuseas y vómitos, cansancio, anemia, infección, dermatitis, acné, disminución del apetito y pérdida de peso, mucositis, sequedad de la piel, astenia.
1. Astenia
Aparece hasta en un 90% de los pacientes con cáncer que están recibiendo tratamiento y puede persistir durante meses o años tras finalizar el tratamiento en más de un 50% de los pacientes. El cansancio asociado al cáncer se define como la sensación de agotamiento físico, emocional y mental persistente que puede estar relacionado con la enfermedad o por sus tratamientos (7). Se describe como una falta de energía que impide realizar pequeños esfuerzos de la vida diaria que no encuentra alivio con el descanso. Puede afectar a la capacidad de trabajar, a la sensación de no sentirse autónomo y a la imposibilidad de compaginar actividades sociales y familiares. En función del tratamiento recibido por el paciente puede aparecer en un momento determinado: a los días de recibir quimioterapia, a las semanas de recibir radioterapia o después de la inmunoterapia.
Existen múltiples escalas para valorar la fatiga en consulta (7), pero aquí se muestran las más utilizadas:
- Rhoten Fatigue Scale: escala numérica del 1 al 10 con un solo ítem.
- FACIT-F: 13 ítems que van de 0 a 4, se puede utilizar de forma independiente pero hay que tener en cuenta que consta de 27 ítems más (FACT-G), y que si se quiere medir la calidad de vida y astenia esta es la escala que ha de ser empleada completa. Consta de 5 dominios: físico, social, emocional, funcional y por último el específico de la astenia. Tiene buena consistencia interna, es fácil y rápida de completar y puede emplearse también en pacientes que no han tenido astenia.
- Brief fatigue inventory (BFI): escala que consta de 9 ítems, utilizada en distintos tipos de pacientes con cáncer y nos va a decir si el paciente está cansado y la severidad de la astenia. Aporta datos sobre la capacidad de relación social y la percepción del propio paciente sobre su astenia. Tiene buena consistencia interna.
- Revised Piper fatigue escale (R-PFS): Es una versión corta de la PFS, consta de 22 Etel (escala analógica visual) y aborda 4 dimensiones de la astenia, la física, la afectiva, la cognitiva y severidad. Deja 4 ítems abiertos para que el paciente indique alguna causa o la duración u otros síntomas. Buena consistencia interna.
- EORTC QLQ-C30: escala multimodal. 30 ítems que incluye una subescala de 3 ítems para medir la astenia. La subescala de 3 ítems, aunque está validada, no se recomienda que se utilice de forma aislada para valorar la astenia. Mide los aspectos físico, social, emocional, cognitivo y funcional. En pacientes en cuidados paliativos se cuestiona su utilización por la dificultad que tiene para saber asignar la respuesta adecuada a la pregunta que se les realiza y por la necesidad del paciente de descansar cuando está realizando el cuestionario.
- ESAS: escala multimodal. Es una de las escalas más utilizadas en la práctica clínica.Se diseñó para pacientes en cuidados paliativos, es de fácil comprensión y realización (5 minutos aproximadamente). Consta de 9 ítems y una décimo para que el paciente escriba algún síntoma específico que no esté dentro de esta. Los 9 ítems son los síntomas más comunes en el paciente con cáncer avanzado, de los 9, seis miden el aspecto físico del paciente y los otros tres el aspecto psicológico. Mide la intensidad de los síntomas con escala analógica visual, cada ítem se puntúa de 0 a 10 (siendo 0 ninguna astenia y 10 mayor astenia que pueda sentir)
Si se conoce la causa de la astenia, se puede realizar un tratamiento dirigido:
-Anemia: corrección de la anemia si la hubiera, cuya etiopatogenia es multifactorial. Se puede producir por pérdidas de sangre agudas o crónicas, hemólisis hipoproliferativa paraneoplásica, por invasión tumoral de médula ósea, neoplasias hematológicas o por carencias nutricionales (déficit de hierro, folato o vitamina B12) (8).
-Hormonas tiroideas: más frecuente en relación al tratamiento con radioterapia, sobre todo en pacientes con cáncer de cabeza y cuello (9).
-Colección de desequilibrios electrolíticos.
Las recomendaciones desde atención primaria para mejorar la astenia son (7):
-Ejercicio físico: el aumento de la actividad física puede reducir el cansancio. Los pacientes con cáncer que realizan ejercicio constante (30 minutos al día o 3-4 horas a la semana) presentan menos astenia y duermen mejor. El ejercicio tiene que ser suave, aeróbico ligero como caminar, bicicleta estática o natación.
-Control nutricional adecuado.
-Medidas psicosociales: reduciendo la tensión, la ansiedad y la depresión se obtiene un efecto beneficioso sobre la fatiga.
2. Náuseas y vómitos
Se presentan en un 50% de los pacientes. Continúan siendo uno de los efectos secundarios que más ansiedad provoca a los pacientes obligando en algunos casos a retrasar tratamientos debido a los efectos secundarios producidos como la deshidratación (10). Atendiendo al régimen de tratamiento: quimioterapia asociada o no a radioterapia. Según las características individuales del paciente:
-Sexo femenino: mayor riesgo de presentar nauseas o vómitos.
-Edad joven.
-Embarazo.
Evolución cronológica:
-Náuseas y vómitos agudos: desde los primeros minutos de la quimioterapia hasta las 24 horas tras el tratamiento. Pico de incidencia las primeras 4-8 horas.
-Náuseas y vómitos diferidos o retardados: a partir de las 24 horas de la administración de la quimioterapia. Incidencia mayor que los agudos (40% de los pacientes), su incidencia y severidad máxima aparece entre las 48-72 horas y pueden durar hasta 6-7 días, en este tipo de vómitos es donde el médico de familia puede prestar más soporte al paciente.
-Náuseas y vómitos anticipatorios: en pacientes que han padecido náuseas y vómitos con ciclos previos de quimioterapia. Aparecen en casi un 30% de los pacientes, son difíciles de controlar, por ello es importante realizar un control de náuseas y vómitos agudos y diferidos desde el primer ciclo de tratamiento.
Dependiendo del grupo farmacológico hay más o menos probabilidad de desarrollar esta complicación, la quimioterapia y la radioterapia son las que más la producen. El tratamiento quimioterápico con cisplatino tiene un riesgo mayor que con carbonoplatino y oxiplatino; presentan riesgo bajo paclitaxel, docetaxel, etoposido, topotecan, pemetrexed, gemcitabina y riesgo mínimo vinorelbina (10).
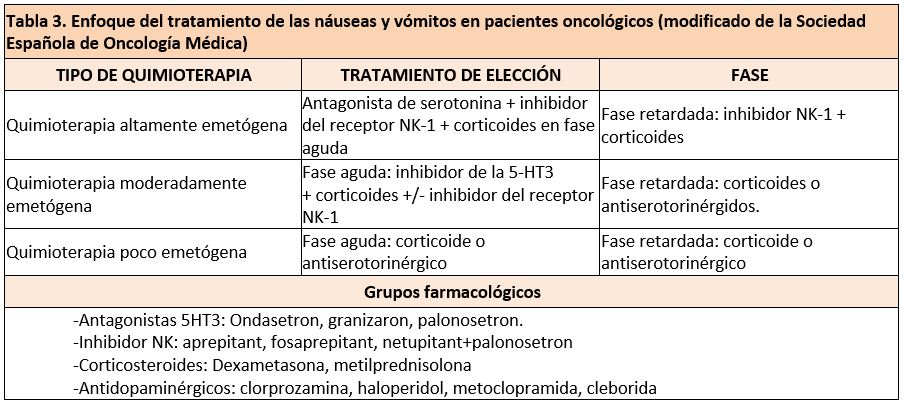
La mejor manera de controlarlos es previniendo su aparición, es recomendable que el paciente anote el número de náuseas y vómitos en un calendario para poder predecir y ajustar el tratamiento necesario. Para el control óptimo se pueden combinar diferentes grupos de fármacos antieméticos en función del poder emetógeno del tratamiento oncológico administrado (10) (tabla 3).
3.Mucositis
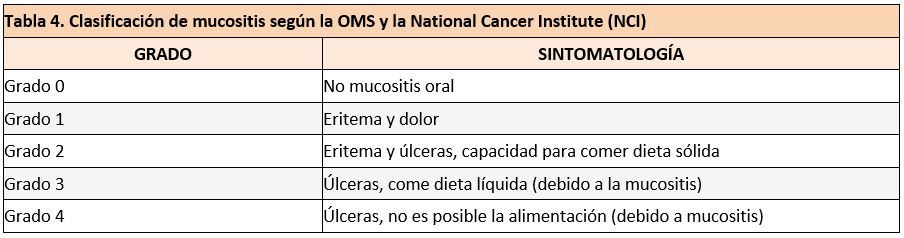
La inflamación y ulceración de la mucosa de la cavidad oral y del resto de tracto gastrointestinal que puede ser causada por la quimioterapia o la radioterapia. Inicialmente suele aparecer sequedad bucal y sensación quemante, pueden evolucionar a dolor severo (11). La clasificación de la mucositis se ofrece en la tabla 4. Se estima que el 20-40% de los pacientes que reciben tratamiento sistémico puede presentar mucositis. Los planes de tratamiento con radioterapia y cisplatino en cánceres de cabeza y cuello pueden presentar mucositis en el 40-80% de los pacientes. Según la Organización Mundial de la Salud (OMS), los pacientes que reciben RT en tumores de cabeza y cuello tienen una intendencia de mucositis oral grado 3 o 4 cercana al 85% (11).
Dependiendo del momento de aparición podemos hablar de: mucositis por toxicidad directa de los quimioterápicos sobre las células de la capa basal de las mucosas (aparece entre la segunda y tercera semana de tratamiento); mucositis por toxicidad indirecta, producida por el efecto citotóxico de la quimioterapia sobre la médula ósea que coincide con el momento nadir de la quimioterapia (7-14 días postquimio), se asocia a neutropenia y su recuperación va asociada al aumento de las cifras de leucocitos. La mucositis suele autolimitarse en el tiempo con una duración media de 14 días. El problema fundamental durante el proceso es la dificultad para la alimentación.
El tratamiento de la mucositis engloba las siguientes acciones (11):
-Higiene bucal con cada comida.
-Enjuagues con anestésicos tópicos como la lidocaína con una dosis diaria no superior a 1,75 mg.
-Fármacos que recubren mucosas.
-Vitamina E (dl-alfa tocoferil acetato) 200-400 mg/día.
-Analgésicos orales.
-Antifúngicos si candidiasis oral (en este caso no utilizar bicarbonato ni clorhexidina por interaccionar con los antifúngicos).
4.Toxicidad cutánea
El 85 % de los efectos secundarios corresponden a erupciones acneiformes, un 15% xerosis, paroniquia, eccema, fisuras, telangiectasias, hiperpigmentación, cambios en el cabello y granuloma piógeno. Aparecen también fenómenos de fotosensibilización, descamación, hiperpigmentación y dermatitis palmo-plantar o síndrome mano-pie (10). No comprometen la vida del paciente, pero tienen un importante impacto en su calidad de vida.
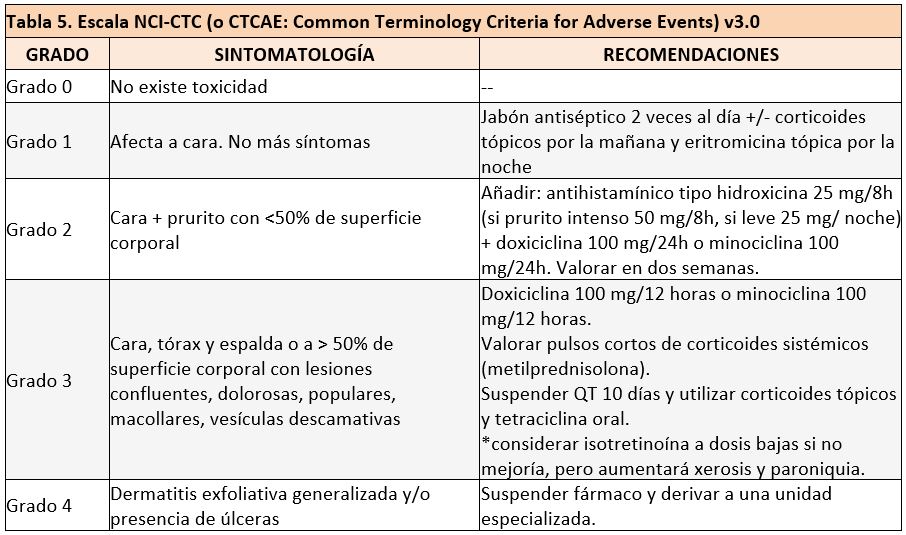
El rash acneiforme o reacción papulopustular, que no es dosis dependiente, se define como una erupción confinada a zonas ricas en glándulas sebáceas como es cara, cuello, zona retroauricular, espalda, parte superior del tórax y cuero cabelludo, pudiendo afectar a otras zonas pero siempre respetando palmas y plantas. Puede haber lesiones hemorragias y costrosas sobre todo en nariz (10). Normalmente se resuelve entre 4-6 semanas quedando importante sequedad cutánea posterior. Para catalogar la severidad de esta toxicidad se emplea la escala NCI-CTC V3 (tabla 5). La cronología de esta toxicidad pasa por distintas fases:
1-Alteración sensitiva con eritema y edema (semana 0-1) en las zonas afectas.
2-Erupción papulopustular (semanas 1-3).
3-Fase de costra (semanas 3-5).
4-Zona de eritemato-telangiectasia.
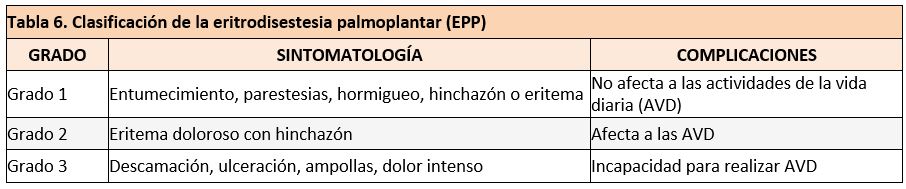
La eritrodisestesia palmoplantar (EPP) se presenta inicialmente como disestesias en palmas y plantas seguido de edema y eritema sistémico, intenso y bien delimitado. Progresa a descamación, ulceración, infección y pérdida de la función en casos graves (tabla 6). Aparece durante las primeras 6 semanas con tratamiento dirigido y durante los dos meses de quimioterapia, es dosis dependiente y más frecuente en mujeres de edad avanzada y con compromiso vascular periférico (12). En los casos leves-moderados se requiere tratamiento sintomático con emolientes como la urea, corticoides tópicos, medidas de soporte físico y en los hábitos de higiene y vestimenta. También se han descrito la utilización de anestésicos locales por vía tópica para el tratamiento del dolor y analgésicos por vía oral. En los casos más severos se describe el uso de vitamina E, inhibidores de la COX-2 y corticoides sistémicos e incluso la disminución de dosis o supresión del tratamiento citostático (13).
La xerosis aparece a las semanas de iniciar el tratamiento, se localiza principalmente en brazos y piernas y en áreas que han sido afectadas por erupción acneiforme. En manos y pies se puede desarrollar una pulpitis seca con fisuras y dolor en los dedos. En tratamiento en preventivo con urea al 5-10% evitando además jabones irritantes y duchas largas, usar agua tibia y evitar cremas muy oleosas por el riesgo de foliculitis. 10
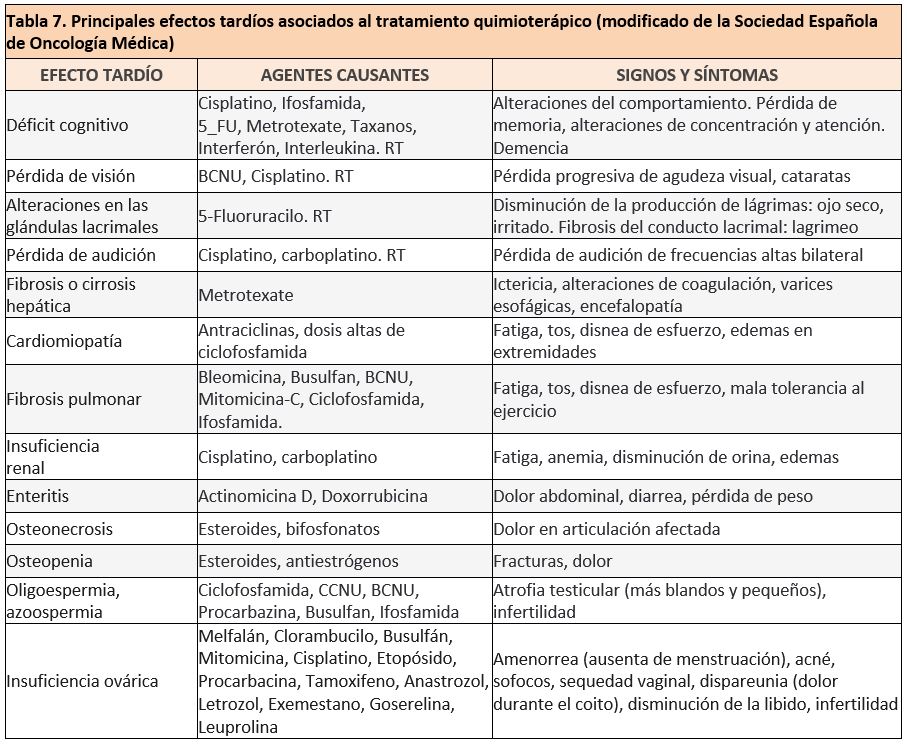
La toxicidad tardía está provocada por el aumento de la supervivencia global de algunas neoplasias, dado que aumenta la esperanza de vida de los pacientes y por ende el aumento de probabilidad de sufrir toxicidad tardía y un aumento de su incidencia es por ello que es de vital importancia el papel del médico de familia para saber reconocerlas, así como un manejo adecuado de las mismas. En la tabla 7 se enumeran los principales efectos tardíos asociados al tratamiento quimioterápico.
TOXICIDADES MÁS COMUNES EN RELACIÓN AL TRATAMIENTO CON RADIOTERAPIA, EL PAPEL DEL MÉDICO DE FAMILIA
Verdú Rotular, Algara López et al. (2002), clasifican las toxicidades del tratamiento radioterápico por aparatos:
1.Astenia
El efecto general atribuible a la radiación. Esta astenia no depende del lugar irradiado ni del tipo de tumor, no se han podido identificar factores etiopatogénicos específicos.
2.Efectos cutáneos
-Alopecia por afectación de las células del folículo piloso. Afectación del área radiada, es irreversible si es mayor a 50 Gy, con menor dosis el pelo puede reaparecer tras el tratamiento, ocasionalmente de textura y color diferente al ocasional.
-Dermatitis aguda: efecto más frecuente de la radioterapia externa. Más frecuente en tumores de mama, pulmón, cabeza y cuello.
El eritema inicial aparece en las primeras 24 horas y alcanza un máximo a partir de la secunda – cuarta semana de tratamiento.
El paciente comienza con prurito por obliteración de glándulas sebáceas, depleción de células proliferativas basales que produce descamación seca, esto puede mantenerse o evolucionar con dolor y edema y continuar su evolución a dermatitis húmeda con vesículas o ampollas, úlceras, hemorragias y necrosis que exija excepcionalmente la suspensión de la radioterapia.
El tratamiento consiste en analgesia, antiinflamatorios y antihistamínicos para el dolor y el, para el prurito se utilizan cremas emolientes, apósitos vaselinados, pomada básica o ungüento emulsionado acuoso.
Si sobreinfección se pautará antibioterapia empírica con amoxicilina/acido clavulánico o cloxacilina.
Durante el tratamiento con radioterapia no se pueden aplican compuestos que contengan metales ya que puede producir un amento de dosis recibida a ese nivel.
3.Efectos orales
-Mucositis: explicada anteriormente. Suele complicarse con sobreinfección por cándida y cede a las 6-8 semanas postratamiento. El 60-90% con RT en tumores de cabeza y cuello presentan mucositis grave.
-Xerostomía: las glándulas salivares son muy sensibles a la irradiación en su aspecto funcional ya durante la primera semana se produce una disminución del flujo de aproximadamente el 50%, que irá disminuyendo con la continuación del tratamiento. La saliva se vuelve densa, pegajosa y viscosa. La xerostomía quedará como secuela irreversible al tratamiento con radioterapia, si bien la mejoría que los pacientes pueden experimentar transcurrido un año. Favorece la sobreinfección sobre todo por cándidas y aumento de la frecuencia de caries. Existen sustitutivos artificiales de saliva.
-Complicaciones orales tardías: la complicación tardía más frecuente es la caries dental secundaria a la disminución y alteración de la saliva, por ello se recomiendan dentífricos ricos en flúor o fluorificaciones. Deberán evitarse las exodoncias de las zonas irradiadas durante el año siguiente al tratamiento por el riesgo de osteoradionecrosis que ello comporta.
4.Efectos digestivos
-Enteritis: necrosis de las células de las criptas que conlleva a la dilatación y atrofia de las vellosidades. Puede ser aguda o crónica. La aguda se inicia a los pocos días de radioterapia en abdomen, pelvis o recto. Puede aparecer malabsorción. Ocurre en el 70% de los pacientes que reciben dosis totales de 50 Gy. En el tratamiento se encuentran medidas como dieta libre de lactosa y grasas, dieta baja en residuos. Entre un 5-15% de los pacientes pueden sufrir enteritis crónica que ocurre al año de la irradiación pero puede aparecer en cualquier momento de la vida del paciente. El tratamiento es el mismos que el de la enteritis aguda pero el 2% precisará abordaje quirúrgico.
-Esofagitis: a las dos semanas de iniciada la radioterapia, aparece como dolor retroesternal, pirosis y disfagia. En pacientes irradiados de cabeza, cuello, pulmón o del aérea esofágica.
-Vómitos: aparecen a las 6-8 horas post irradiación pero la sensación nauseosa puede aparecer en las primeras dos horas.
5.Efectos genitourinarios
-Cistitis: afecta al 37% de los pacientes irradiados por adenocarcinoma de próstata. La cistitis hemorrágica puede aparecer tras más de tres años terminada la radioterapia.
-Impotencia: aparece en el 30-70% de los pacientes irradiados en región pélvica. Si no hay contraindicación el tratamiento de elección es el sildenafilo o inyecciones intracavernosas de alprostadil y las cámaras de vacío.
-Disfunción hormonal: se puede producir pérdida de la función gonadal con la irradiación de la región pélvica con una dosis entre 5-20 Gy, una dosis de 30 Gy puede producir menopausia en un 60% de las mujeres. Se puede producir estenosis vaginal. Evitar el embarazo durante un año posterior al tratamiento.
La afectación en el ovario se presenta de forma diferida, mientras que en el testículo se presenta de forma aguda produciendo necrosis de espermatogonias y células germinales (si dosis menor de 5 Gy no son permanentes, produciéndose una oligospermia temporal que puede durar semanas o meses).
Bibliografía
- (2024, 26 de enero). Las cifras del cáncer en España 2024. Recuperado de REDECAN. Disponible en: https://www.redecan.org .
- López Verde F. El médico de familia en la atención al paciente con cáncer. Elsevier.2016; 48(5): 277-278
- Guillén Ponce C, Molina Garrido MJ. Qué es, cómo funciona y tipos de quimioterapia [Internet]. SEOM. 2023. [febrero 2023] disponible en: https://seom.org/guia- actualizada-de-tratamientos/que-es-como-funciona-y-tipos-de-quimioterapia
- Zamora P. Hormonoterapia o tratamiento hormonal [internet]. SEOM. 2020 [enero 2020] disponible en: https://seom.org/guia-actualizada-de-tratamientos/que-es-y- como-funciona-la-hormonoterapia
- Remon J. La inmunoterapia del cáncer [Internet]. SEOM. 2022. [diciembre 2022]. Disponible en: https://seom.org/guia-actualizada-de-tratamientos/la-inmunoterapia-del- cancer
- Urruticoechea A, Hernández Jorge A. Tratamiento biológicos: qué son y cómo actúan. [Internet] SEOM. 2019. [diciembre 2019] disponible en: https://seom.org/guia- actualizada-de-tratamientos/nuevos-tratamientos-biologicos-que-son-y-como-actuan
- San-Miguel Arregui MT, Bruera E. Evaluación multidimensional de la astenia relacionada con el cáncer. Med Paliat. 2014; 21(1): 21-31
- Mañas MD, Lázaro C, Galiana J, et al. Características de la anemia en los pacientes oncológicos en tratamiento paliativo. 2015; 22(3): 100-105
- Ferrer JC, Massó MF, Alba JR. Et al. Hipotiroidismo primario postradioterapia en pacientes con cáncer de cabeza y cuello. Elsevier. 2005;52(8): 387-390
- Blasco A, Caballero C. Toxicidad de los tratamientos oncológicos. SEOM. 2019 [diciembre 2019]. Disponible en: https://seom.org/guia-actualizada-de-tratamientos/ toxicidad-de-los-tratamientos-oncologicos
- Jeldres M, Amarillo D, Lorenzo F, García F, Cuello M. Patogenia y tratamiento de la mucositis asociada al tratamiento de radioterapia y/o quimioterapia en pacientes con cáncer de cabeza y cuello. Rev Urug Med Int. 2021; 6(1): 4-13
- González Freire L, Boullosa Sale S, Dávil Pousa MC, Crespo-Diz C. Tratamiento de la eritrodisestesia palmoplantar con una fórmula magistral de urea 20% + triamcinolona acetónido 0,2% + lidocaína 2%. Rev. OFILILAPHAR 2022; 32(3):301-303.
- Reyes Herrera A. Eritrodisestesia palmoplantar por capecitabina, en una mujer con cáncer de mama. Dermatol Rev Mex. 2012; 56(1):71-3.
- Verdú Rotellar JM, Algara López M, Foro Arnalot P, Domínguez Tarragona M, Blanch Mon A. Atención a los efectos secundarios de la radioterapia. Medifam [Internet]. 2002; 12(7): 16-33. Disponible en: http:// isciii.es/scielo.php?script=sci_arttext&pid=S1131-57682002000700002&lng=es.
